Omics technikák: mérjünk mindent egyszerre
Az „omics” gyűjtőfogalom olyan módszerekre, amelyek egyszerre több ezer komponenst mérnek. Nagy áteresztőképességű molekuláris térképezés, mely előbb üt, aztán kérdez. Azaz rengeteg adatot gyűjt be, majd utána big-data elemzésekkel feltárja az összefüggéseket.
• genomika – teljes DNS
• transzkriptomika – összes mRNS
• proteomika – összes fehérje
• metabolomika – anyagcsere-molekulák
• lipidomika – lipidfajták profilja
• epigenomika – kromatinállapot, DNS-reguláció
Miért fontosak az omics technikák az idegtudományban?
A klasszikus módszerekkel csak egy-egy génre vagy fehérjére tudtunk fókuszálni.
Az agy azonban nem így működik: rendszerek, hálózatok, sejtprogramok állnak össze a viselkedés mögött. A modern omics és multiomics technikák lehetővé teszik, hogy:
egyetlen sejtről több száz vagy ezer adatot kapjunk, az anatómiai helyzettel összevethető molekuláris térképeket készítsünk, a környezeti hatások (stressz, drogok, traumák, tanulás) okozta változásokat, szabályozómechanizmusok szintjén értsük meg.
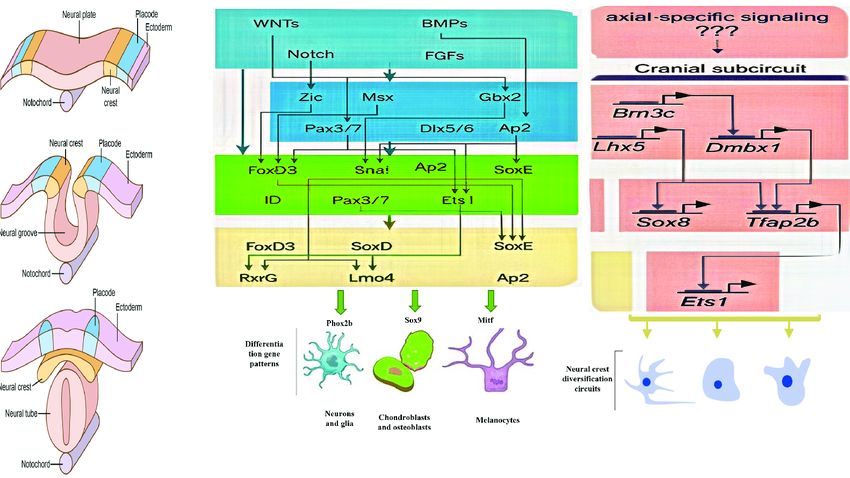
Bulk és egysejt-transzkriptomika (scRNA-seq)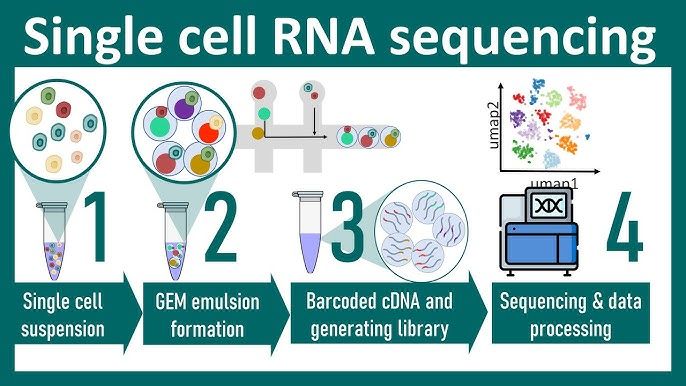 Ennek a tébeli felbontása ez előzőnél finomabb. A technikával egyedi sejtek génexpressziós mintázatát tudjuk meghatározni. Nincs többé „átlagos molekuláris jel” egy agyterületből, helyette minden sejt külön molekuláris ujjlenyomatot kap. Különböző neuron- és gliasejttípusokat azonosíthatunk, megtudjuk fejlődési
Ennek a tébeli felbontása ez előzőnél finomabb. A technikával egyedi sejtek génexpressziós mintázatát tudjuk meghatározni. Nincs többé „átlagos molekuláris jel” egy agyterületből, helyette minden sejt külön molekuláris ujjlenyomatot kap. Különböző neuron- és gliasejttípusokat azonosíthatunk, megtudjuk fejlődési 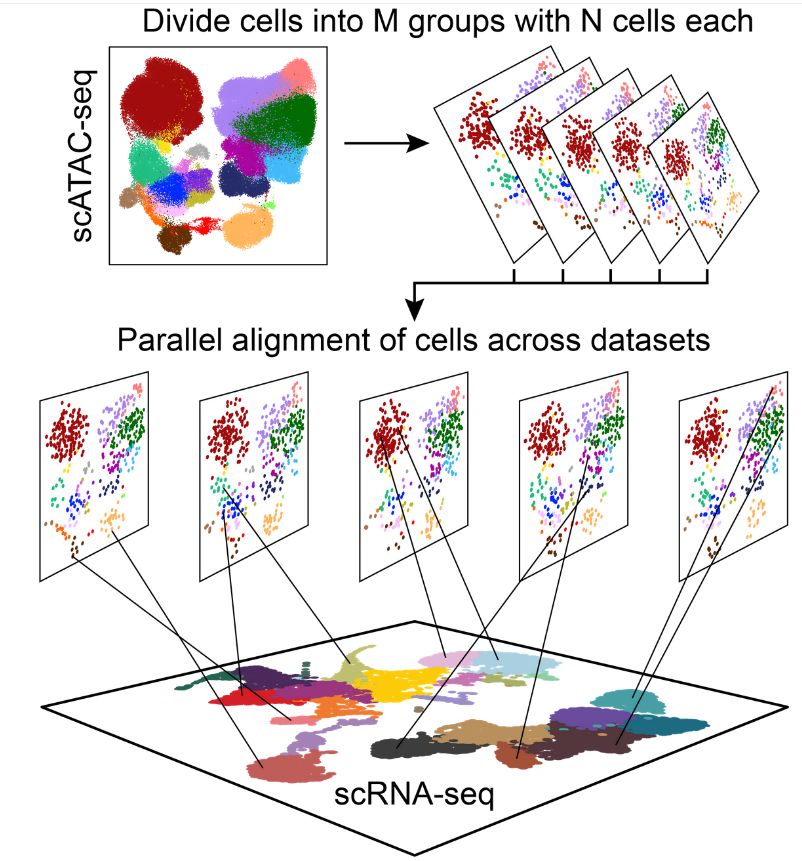 vonalaikat, érési folyamataikat. Megnézhetjük, hogy a tanulás, stressz, drogok hogyan módosítják az egyedi sejttípusok génaktivációját. Kereshetünk kóros sejttípusokat pl. epilepsziában, neurodegenerációban. A scRNA-seq lett az elmúlt 10 év legfontosabb sejtbiológiai technikája. A módszert bemutató YouTube videó (angolul).
vonalaikat, érési folyamataikat. Megnézhetjük, hogy a tanulás, stressz, drogok hogyan módosítják az egyedi sejttípusok génaktivációját. Kereshetünk kóros sejttípusokat pl. epilepsziában, neurodegenerációban. A scRNA-seq lett az elmúlt 10 év legfontosabb sejtbiológiai technikája. A módszert bemutató YouTube videó (angolul).
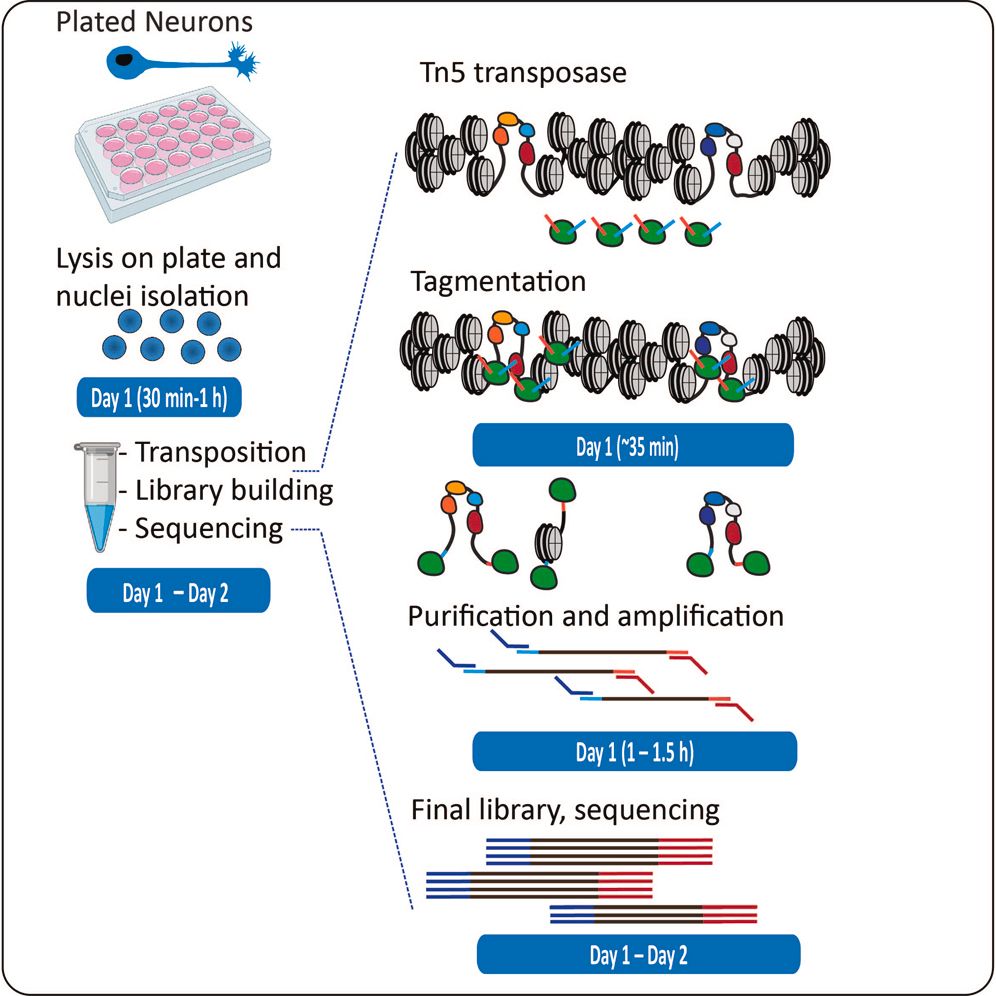
ATAC-seq – A kromatin nyitottságának mérése
Az ATAC-seq azt mutatja meg, mennyire hozzáférhető a DNS a szabályozó fehérjék számára. Ez a génaktiváció alapja, ugyanis a génátíráshoz a DNS bizonyos szakaszainak ki kell tekerednie (nyitott kromatin). A zárt, csomagolt régiók nem olvashatók – ezek inaktívak. Az ATAC-seq tehát egyfajta epigenetikai feltérképezés, ami megmutatja: mely gének potenciálisan bekapcsolhatók, hol vannak enhancer vagy promoter régiók aktív állapotban, hogyan változik a kromatin stressz, tanulás vagy drogok hatására.
scRNA-seq + ATAC-seq kombinációja: Génexpresszió és epigenetika egyszerre
Ez az irány gyakran „multiomics single-cell profiling” néven fut.
A scRNA-seq (single cell, egysejt szekvenálás) megmondja milyen gének aktívak egy sejtben, az ATAC-seq pedig hozzáteszi miért aktívak (milyen epigenetikai állapot teszi lehetővé). Így a génexpressziós változások okai is vizsgálhatók, a környezeti hatások (stressz, droghasználat, tanulás) által kiváltott változások molekuláris mechanizmusa feltárható, a sejtállapotok precízen kategorizálhatók. Ez a módszer jelenleg a legmélyebb betekintést adja a komplex idegrendszeri adaptációkba.
Proteomika – az összes fehérje mérése
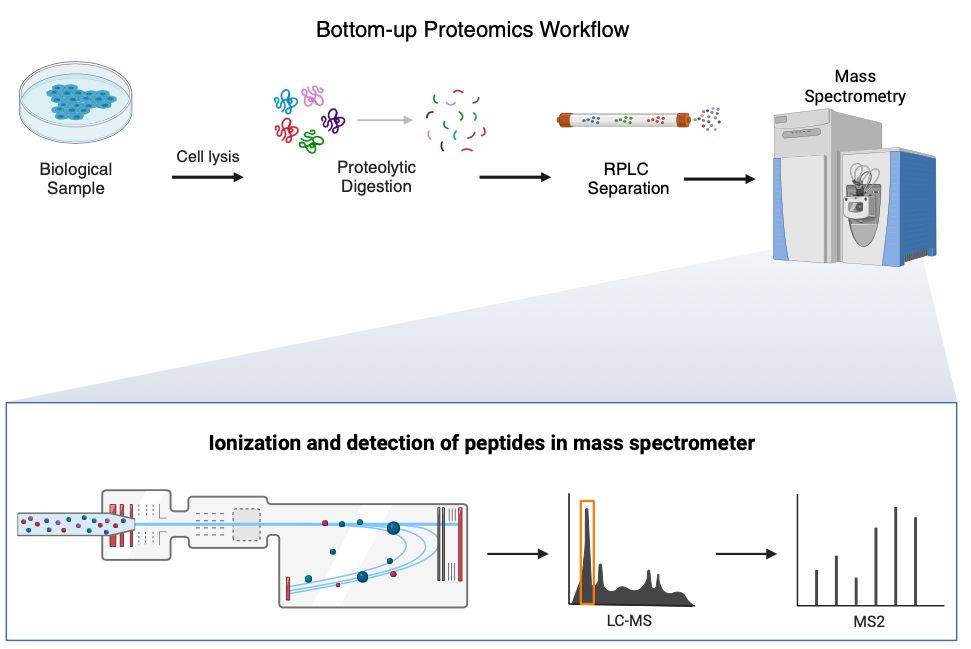
Az ATAC-seq azt mutatja meg a genom mely része írható át, a transzkriptom azt mutatja, milyen mRNS van jelen (azaz valóban mi jródhat át ), a proteomika azt, hogy ebből milyen fehérje keletkezik ténylegesen. Mivel az mRNS-ek átirásának is vannak szabályozó rendszerei, ezért fontos tudni mely mRNSkből lesz az adott állapotban fehérje, az igazi végrehajtó molekula. A kettő között gyakran nagy a különbség, ezért fontosak a proteomikai mérések. A mérések során a mintát először tripszinnel megemésztik aminek hatására a fehérjék jellegzetes polipetid darabokra esnek szét. Minden fehérjére jellemző egy polipeptid mintázat. Ezeket a darabokat két lépcsős tömeg spektrometriával elezik, melynek során a peptideket súlyuk és elektromos töltésük arányának nagyon finom eltérései alapján azonosítják. Utána adatbázis feldolgozó módszerekkel azonosítják, hogy a peptid darab eloszlás alapján milyen eredeti fehérjék azonosíthatók.
Modern irányok: térbeli proteomika – hol vannak a fehérjék a szövetben, időbeli proteomika – hogyan változnak gyors folyamatok alatt.
Lipidomika – a sejt zsírkomponenseinek mérése
A lipidek (zsírok) nem csak energiatárolók, hanem:
• sejthártya építőkövei,
• jelátviteli molekulák,
• neuromodulátorok,
• gyulladásos válaszok kulcselemei.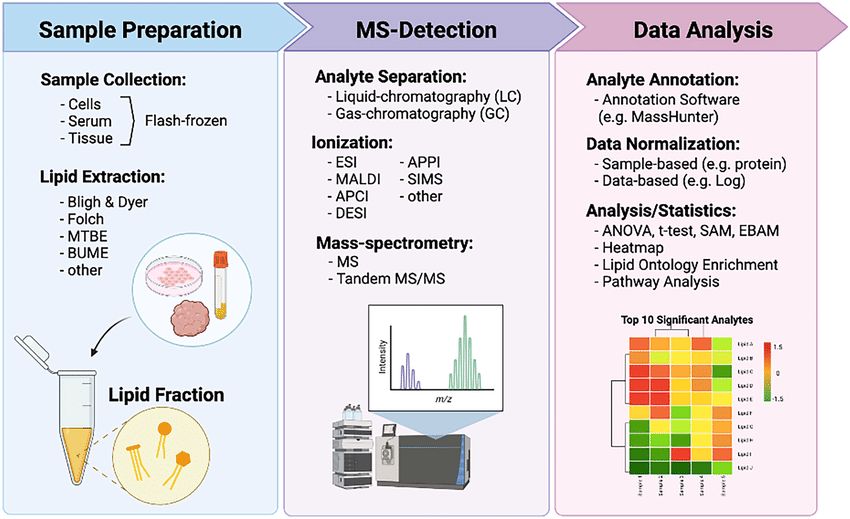 A lipidomika az agyban különösen fontos, mert a membránok összetétele szabályozza a receptorok működését, az axonok szigetelésében fontos mielinhüvely zsírokban gazdag, neurodegenerációban a lipidanyagcsere zavara korai jel. A legújabb módszerek már térben is képesek lipidfajtákat lokalizálni, azaz nem csak azt mondják meg, hogy egyfajta zsír előfordul, hanem azt is hol.
A lipidomika az agyban különösen fontos, mert a membránok összetétele szabályozza a receptorok működését, az axonok szigetelésében fontos mielinhüvely zsírokban gazdag, neurodegenerációban a lipidanyagcsere zavara korai jel. A legújabb módszerek már térben is képesek lipidfajtákat lokalizálni, azaz nem csak azt mondják meg, hogy egyfajta zsír előfordul, hanem azt is hol.
Ezekkel a módszerekkel az idegtudomány egy új korszakba lépett. Az agy működését már nem csak elektromosan vagy anatómiailag, hanem molekuláris hálózatokként is tudjuk vizsgálni.
Szerző: Gulyás Attila





